Kinderwunsch I Endokrinologie
Syndrom der Polycystischen Ovarien, PCO, PCOS
Auch wenn die Ursachen bis heute nicht vollständig geklärt sind: Eine Behandlung des PCO S ist insbesondere bei Kinderwunsch gut möglich.
Biologisch ganze Sicht
Da wir das PCO Syndrom nicht (mehr) ausschließlich als endokrin-metabolisches Syndrom betrachten, sondern auch als autoimmun - entzündliches Geschehen des gesamten Menschen, in der Regel findet sich ja eine Symptomenkomplex, behandeln wir das PCO Syndrom in unserer Praxis seit mehr als 20 Jahren auch nach integralmedizinischen Prinzipien. Der Mensch wird betrachtet, behandelt und nicht ausschließlich das Organ und das Symptom.
Literatur: u.a. Inflammation in Polycystic Ovary Syndrom. Underpinning of insulin resistance and ovarian dysfunction. F. Gonzales, M.D., Steroids, 2012 March 10; doi: 10.2016/j.steroids. 2011.12.003
PCOS: Ursachen, Diagnostik , Therapien
Auch schlanke Frauen sind betroffen
Entgegen der häufigen Annahme, das PCOS trete nur bei Frauen mit Übergewicht auf, betrifft das PCOS auch schlanke Frauen. Auch hier zeigen sich zum Beispiel bestimmte Hormonwerte erhöht (LH), während diese bei übergewichtigen Frauen gar normal sein können. Daher gilt der erhöhte LH/FSH-Quotient > 3:1 als Hinweis, aber nicht mehr als entscheidendes Kriterium in der Diagnose des PCOS.
Übergewicht / Insulinüberschuss durch Insulinresitenz
Schlanke Frauen mit PCOS haben in der Regel allerdings keine Zuckerstoffwechselstörung (Hyperinsulinämie) und keine Insulinresistenz. Bei übergewichtigen Frauen steigt die Wahrscheinlichkeit einer Insulinstoffwechselstörung hingegen mit zunehmendem Gewicht an.
Mit dem oralen Glucose-Toleranztest, OGGT, lässt sich eine Zuckerstoffwechselstörung, die Hyperinsulinämie gut und verhältnsimässig einfach nachweisen.
Auch klinische Befunde alleine lassen eine Insulinresistenz mit Hyperinsulinämie wahrscheinlich erscheinen. Dazu gehören z.B. ein Body Maß Index (BMI) von mehr als 27, ein Taillen Hüftumfang Verhältnis von größer als 0,85, ein Taillenumfang von mehr als 100 cm, eine Akanthosis nigricans, dunkle Hautpigmentierungen, Verhornungen an spezifischen Körperstellen und multiple Akrochordons, sog. Saiten-, oder Stielwarzen.
Die Hyperandrogenämie mit Insulinresistenz und Akanthosis nigricans ist eine Form des PCOS mit schwerer Insulinresistenz, die auf einer Mutation des Insulinrezeptor Gens beruhen kann. Eine Akanthosis nigricans ist praktisch beweisend für eine Insulinresistenz, jedoch haben viele Frauen mit PCOS und Insulinresistenz keine Akanthosis nigricans. Die Diagnose selbst ist also nicht immer eimdeutig.
Bezogen auf den BMI lässt sich aus gynäkologischer Sicht die allgemeine Annahme treffen: Bei einem BMI von kleiner 22 besteht keine Insulinresistenz, bei einem BMI von größer 27 besteht wahrscheinlich und bei einem BMI von größer 30 mit großer Sicherheit eine Insulinresistenz. Die Bedeutung der Insulinresistenz beim PCOS besteht zum einen darin, daß diese Frauen gefährdet sind, einen Diabetes mellitus Typ 2 zu entwickeln und verstärkte kardiovaskuläre Risiken aufweisen. Zum anderen ist die Insulinresistenz bei dieser Unterform des PCOS an der Entwicklung des Syndrom zumindest beteiligt. Dies bedeutet, daß eine therapeutisch günstige Beeinflussung der Insulinresistenz gleichzeitig eine Behandlung des PCOS bei Hyperinsulinämie darstellt und günstige Voraussetzungen für eine erfolgreiche Sterilitätstherapie schafft.
Diagnose des PCO
Es gibt keine sicheren Zeichen eines PCO-Syndroms. Die Diagnostik des PCOS ist daher ein Mosaik verschiedener Parameter und unterliegt der erfahrenen zusammenfassenden Bewertung.
• Zyklusbestimmung
• BMI < 22 keine Insulinresistenz
• BMI 22 - 27 unwahrscheinliche Insulinresistenz
• BMI > 27 wahrscheinliche Insulinresistenz
• BMI > 30 sichere Insulinresistenz
• Blutbestimmungen. Neben den erhöhten Androgenspiegeln finden sich häufig erhöhte LH- und normale FSH-Spiegel mit einer erhöhten LH/FSH Ratio. Eine gesteigerte hypothalamische Aktivität, Störungen in der ovariellen und adrenalen Steroidhormon Synthese und Störungen des Insulinstoffwechsels werden zumindest diskutiert. Testosteron, Androstendion, Dehydroepiandrosteron-Sulfat und eine Oligo-Amenorrhoe sind einige endokrinologische Parameter des PCOS, wenn sie nicht durch einen Androgene produzierenden Tumor oder einen Nebennieren -rindenenzymdefekt verursacht sind. Ebenso LH und FSH, wobei der LH/FSH Quotient eben ist nicht zwingend erhöht sein muss.
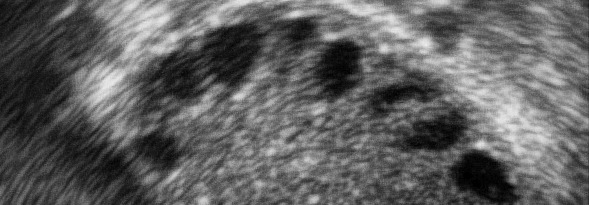
Ultraschall
Auch wenn sich im Vaginalultraschall als Hinweis häufig die typischen PCO - Ovarien mit dem vermehrten zentralen Stroma und den randständigen multiplen perlschnurartig aufgereihten kleinen Follikelzysten finden, so gilt dieser Befund heute nicht mehr primär zu den Kriterien des PCOS, auch wenn die klinische Erfahrung dies dennoch häufig in den diagnostischen Vordergrund stellt.
Therapien PCOS
Es bieten sich in Abhängigkeit von den Beschwerden eine Reihe von Therapien. Die derzeit praktizierten therapeutische Ansätze richten sich aber vor allem nach der im Vordergrund stehenden klinischen Symptomatik. Dies ist in eine bio.logischen Betrachtung allerdings nicht ausreichend.
Operative Therapien
Operative Verfahren wie die Keilresektion der Ovarien, die erstmals 1935 von Stein und Leventhal beschrieben wurden, werden nur noch sehr selten angewandt. Heute wird ggf. die Minilaparotomie favorisiert. Die Laserbehandlung der Ovarien kann in manchen Fällen von Nutzen sein. Minimal invasive chirurgische Verfahren wie z.B. die transvaginale Hydrolaparoskopie sind in Erprobung, zählt aber zu den symptomatischen Therapien.
Hirsutismus & Zyklusstörungen
Hierzu werden vor allem Ovulationshemmer eingesetzt. Im Falle der Aknetherapie werden Präparate mit höherem Östrogen - und spezifischem Gestagenanteil empfohlen. Eine Verbesserung des Hirsutismus kann in einigen Fällen auch durch den Einsatz von Spironolacton erreicht werden, dabei ist jedoch ein Konzeptionsschutz zur Vermeidung fetaler Missbildungen allerdings unerlässlich. Niedrig dosierte Glukokortikoide können in Einzelfällen zur Hemmung der adrenalen Steroidsynthese genutzt werden. Die Kombination von Spironolacton mit Steroiden soll die Remissionsphase des Hirsutismus verlängern. Bei Adipositas ist eine Reduktionsdiät anzustreben, die jedoch nur von wenigen Patientinnen dauerhaft durchgehalten wird (5-10% über 5 Jahre). Insofern halten wir dies nicht für einen Primäransatz, wie auch die medikamentösen Strategien.
Neue Therapieansätze bei Hirsutismus, Akne, Alopezie
Finasterid, ist ein 5-alpha Reduktase Inhibitor, ist in Deutschland in der Behandlung des Hirsutismus bislang nicht zugelassen ist. Internationale Studien belegen allerdings einen positiven Effekt auf den Hirsutismus bereits nach 6 Monaten Therapie.
Flutamid, ein potentes Antiandrogen, zeigte in Studien eine moderate Besserung der Alopezie nach 12 monatigem Einsatz eine positive Beeinflussung des Hirsutismus (Carmina et al. 2003). Auch dieser Wirkstoff ist für Frauen derzeit nicht zugelassen. Hinsichtlich der Akne zeigt Flutamid ähnlich gute therapeutische Effekte wie eine antiandrogene Ovulationshemmer Therapie.
Neuere orale Kontrazeptiva, bestehend aus Ethinyl Östradiol und Drospirenon konnten ebenfalls effektiv in der Behandlung der moderaten Akne eingesetzt werden.
Kinderwunsch
Bei Kinderwunsch sollte bis auf wenige Ausnahmen (z.B. M. Hashimoto) eine kontinuierliche Einnahme von Folsäure und Jod erfolgen. Eine Vorbehandlung ist mit einer antiandrogenen Pille und / oder Glukokortikoiden möglich. Niedrig dosierte Glukokortikoide, täglich morgens können zur Hemmung der Steroidsynthese in der Nebenniere genutzt werden. Darüber hinaus können sie die Einnistung des Embryo günstig beeinflussen.
Clomifen. Clomifen wird seit 1967 in Deutschland zur Ovulationsinduktion eingesetzt und bewirkt einen Eisprung bei bis zu 8 von 10 Frauen. Die Schwangerschaftsrate kann dann bei bis zu 20 - 50% liegen kann. Zu beachten ist: Die Behandlung geht mit einem erhöhten Risiko von Mehrlingsschwangerschaften (ca. 10-20%) einher. Deswegen ist Dosisfindung und eine engmaschige Überwachung durch erfahrenen gynäkologischen Ultraschall unerlässlich. Eine - wie häufig früher erfolgt - unkontrollierte Gabe führt ggf. zu hohen Mehrlingsschwangerschaften mit bis Fünf- und Sechslingen. Die ovarielle Stimulation des beim PCOS ist eine nicht immer einfache Behandlung, die eine engmaschige Kontrolle erfordert.
Clomiphen darf bislang nur über einen Zeitraum von insgesamt 6 Zyklen erfolgen, da sonst gegebenenfalls das Risiko steigen kann an einem Ovarialkarzinom zu erkranken. Nach der sechsmaligen Clomifenbehandlung kommen dann Gonadotropine zum Einsatz. Hierbei sind Kombinationen aus FSH und LH oder FSH-Monopräparate erhältlich. Die Anwendung sollte erst nach erfolgloser Clomifenbehandlung erfolgen und bedarf einer engmaschigen Kontrolle. Gleichzeitig sollte bei der Clomifenbehandlung eine vaginale Hormonbehandlung erfolgen, da Clomifen als Antiöstrogen ggf. ungünstige Effekte auf den Cervixschleim haben kann, was das Aufsteigen der Spermien in die Gebärmutter behindern kann.
Auslösung des Eisprungs: Als wichtigste Nebenwirkung wird bei dieser Therapieform die Überstimulation angesehen. Im Falle eines Therapieversagens bleibt einigen Patientinnen als ultima ratio nur noch die In-Vitro-Fertilisation (IVF). Gelbkörperstützung. 2-3 Tage nach der Auslösung sollte Gelbkörperhormon vaginal mit 2x1 täglich verabreicht werden.
Insulinresistenz - Metabolisches Syndrom
Auch wenn die Insulinresistenz nicht die alleinige Ursache für die Entstehung eines PCOS darstellt, so verstärkt die begleitende Hyperinsulinämie durch eine Steigerung der ovariellen und adrenalen Androgenproduktion den Circulus Vitiosus des PCOS. Das Verständnis dieser Zusammenhänge führte zum Einsatz der Insulinsensitizer in der Behandlung betroffener Frauen.
Internationale Studien zeigten unter Therapie mit Metformin eine signifikante Senkung der Androgene, eine Erhöhung des SHBG und eine Normalisierung des Menstruationszyklus mit Verbesserung der Fertilität (Diamanti et al. 1998, Moghetti et al. 2000, Velazquez et al. 1994). Obwohl unter Metformintherapie eine signifikante Senkung der laborchemischen Hyperandrogenämie erreicht wurde und sich eine deutliche Besserung der Akne fand, zeigte sich der Hirsutismus-Score in vielen Fällen nur moderat gesenkt.
Als mögliche Erklärung kann eine erhöhte 5-a-Reduktase Aktivität in der Haut angenommen werden. Der offensichtlich bessere Effekt der Ovulationshemmer, insbesondere mit antiandrogener Komponente, auf den Hirsutismus wird jedoch mit einer Verschlechterung der metabolischen Parameter un einer zumeist passageren Gewichtszunahme erkauft (Morin-Papunen et al. 2003). Positive Effekte der Metformin-Therapie lassen sich auch in Kombination Ethinyl-Östradiol/Cyproteron-Acetat (Elter et al. 2002) oder mit Clomiphen dokumentieren (Nestler et al. 1998). Erste Daten belegen, dass auch nicht-insulinresistente PCOS-Patientinnen von einer Metformintherapie profitieren.
Ähnliche Effekte wurden in klinischen Studien für die Glitazone (Rosiglitazon, Pioglitazon, Troglitazon) gezeigt. Orale Antidiabetika und somit auch Metformin werden allgemein als potentiell teratogen und in der Schwangerschaft als kontraindiziert angesehen. Eine Fortführung der Metformingabe in der Schwangerschaft ist zur Zeit Gegenstand kontroverser Diskussionen. Erste Studien zum Einsatz von Metformin bei schwangeren PCOS-Frauen ergaben keine erhöhte Rate an Entwicklungsverzögerungen oder Missbildungen der Feten (Glueck et al. 2002). Es zeigt sich jedoch eine Reduzierung der Gestationsdiabetes-Fälle und eine signifikante Senkung der Frühabortrate von 62% auf 26%.
Metformin verbessert erwartungsgemäß auch die Parameter des Metabolischen Syndroms, insbesondere die Insulinresistenz. Besonders hervorzuheben ist auch die Gewichtsabnahme bei vielen PCOS-Patientinnen, im Mittel etwa 6 - 10 kg in 6 Monaten. Zudem ergibt sich eine Senkung der Triglyceride, des systolischen Blutdrucks und eine Erhöhung des HDL-Cholesterins. Eine Zusammenstellung der Metformin-Daten findet sich auch im Cochrane Review 2003 der Cochrane Library.
Letrozol vs. Clomifen
In einer aktuellen grossen Studie untersuchten und verglichen die Autoren die Substanzen Letrozol mit Clomifen bei Frauen mit unerklärter Unfruchtbarkeit. Sie kommen nach Durchsicht aller randomisierten Studien zu dieser Fragestellung zu dem Schluss, dass Letrozol nicht nur gleich wirksam wie Clomifen ist, sondern es sogar zu einer Zunahme der erzielten klinischen, weiterführenden Schwangerschaftsraten kommt. Offenbar führt Letrozol im Vergleich zum Einsatz von Clomifen zu einer Reduktion von Schwangerschaftsfehlanlagen. Letrozol ist für die Homonbehandlung bei unerfülltem Kinderwunsch allerdings nicht zugelassen ist. Es handelt sich damit um einen individuellen„Off Label Use“.
Bitte beachten sie: Es handelt sich in dieser Publikation um allgemeine Empfehlungen, aktuelle Forschung und ggf. neue Therapieansätze, die teils im sog. Off-label-Use immer mit einem in der Behandlung des PCOS erfahrenen Arzt individuell abgestimmt werden müssen.
Literatur (Auswahl)
Barbieri RL (2000) Induction of ovulation in infertile women with hyperandrogenism and insulin resistence. Am J. Obstet. Gynecol. 183: 1412-1418
Vandermolen DT, Ratts VS, Evans WS, Stovall DW, Kauma SW, Nestler JE (2001) Metformin increases the ovulatory rate and the pregnancy rate from clomiphene citrate in patients with polycystic ovary syndrome who are resistant to clomiphen.
Liu A. et al. Letrozole vs. Clomifencitrate for unexplained infertility: a systematic review and metaanalysis. J Obstet Gynaecol Res 2014; 40 (5): 1205-16